又有生物科技企业向港股发(fa)起冲击。
格隆汇新股获(huo)悉,近期,劲方医药科技(上海)股份有限企业-B(以下简称“劲方医药”)向港交所(suo)递交了招股书,中信证券担任保(bao)荐人。
劲方医药成立于2017年,是一家处于市场化(hua)阶段的生物制药企业,专注于肿瘤(liu)、自(zi)体免疫和炎症性疾病(bing)领域的创新及有效治疗方案。
2021年,企业与信达生物就核心管线KRASG12C抑制剂氟泽雷塞片达成合作,交易总(zong)额超过3亿美金,在(zai)当时引起了不小(xiao)的轰动。
劲方医药由两位联合创始人领导,分别是吕强博士和兰炯博士。吕强博士担任董事长兼实行董事,兰炯博士担任首席实行官(guan)兼实行董事,两位创始人在(zai)生物医药领域均拥有丰富(fu)的经验。劲方医药的研(yan)发(fa)团(tuan)队有61人,其中17人拥有博士学位。
自(zi)成立以来,劲方医药完成了多轮融资,累计融资金额超过人民币14.21亿元,其中C+轮融资的投后估值为31.24亿元。
企业吸(xi)引了多位知名投资者押注,包括弘晖资本、华盖资本、亚(ya)投资本、百度风投、深创投、石药集团(tuan)等。
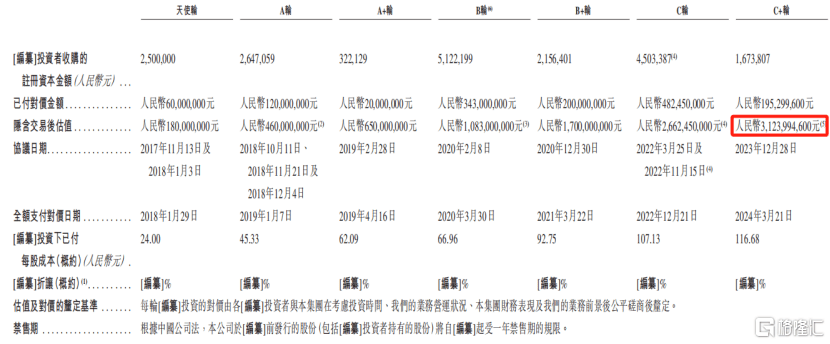
企业融资历程,来源:招股书
截至2024年12月21日(ri),企业已建立起一条持续更新的产品管线,包括八款候(hou)选药品,其中五款处于临床开发(fa)阶段,一款已经获(huo)批上市,还有2款出于临床前(qian)研(yan)发(fa)阶段。
企业通过与信达生物、SELLAS等合作伙伴的紧密合作,加速(su)了核心产品的临床开发(fa)和商业化(hua)进程。核心产品GFH925已在(zai)中国实现(xian)商业化(hua),而GFH312等产品正(zheng)在(zai)全球(qiu)范围内推进临床试验。
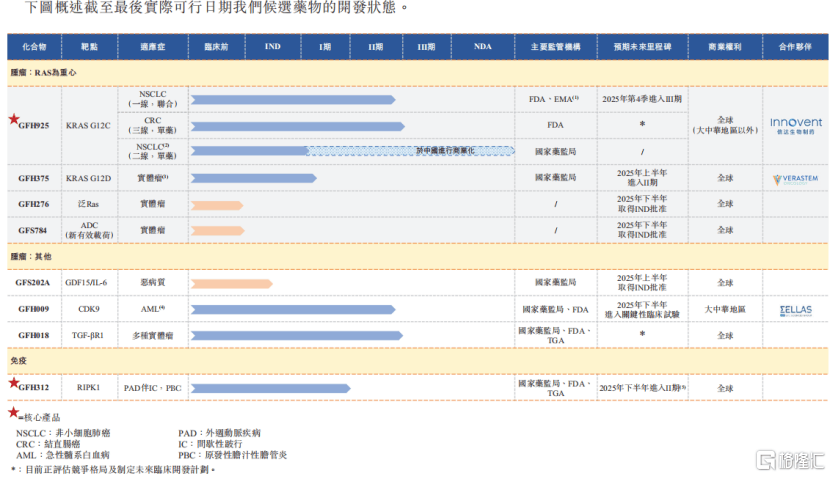
企业管线产品,来源:招股书
核心产品:
GFH925(商品名达伯特(te))是一款自(zi)主(zhu)研(yan)发(fa)的小(xiao)分子KRAS G12C抑制剂。2024年8月,该药物获(huo)中国国家药监(jian)局批准上市,并被认(ren)定(ding)为突破性疗法。截至2024年12月21日(ri),GFH925的专利期限超过15年。
作为治疗KRASG12C突变的非小(xiao)细胞肺癌(ai)(NSCLC)的二线或后线疗法,GFH925是中国首款、全球(qiu)第三款获(huo)批的KRASG12C抑制剂。
目前(qian),劲方医药正(zheng)在(zai)推进GFH925的海外临床开发(fa),以释出其治疗潜力,包括作为一线疗法与cetuximab联合用(yong)于治疗晚期NSCLC的Ib/II期临床试验,以及作为单(dan)药疗法用(yong)于治疗难治性转移性CRC的后线疗法。
从行业来看,NSCLC及CRC均有较大的治疗市场。
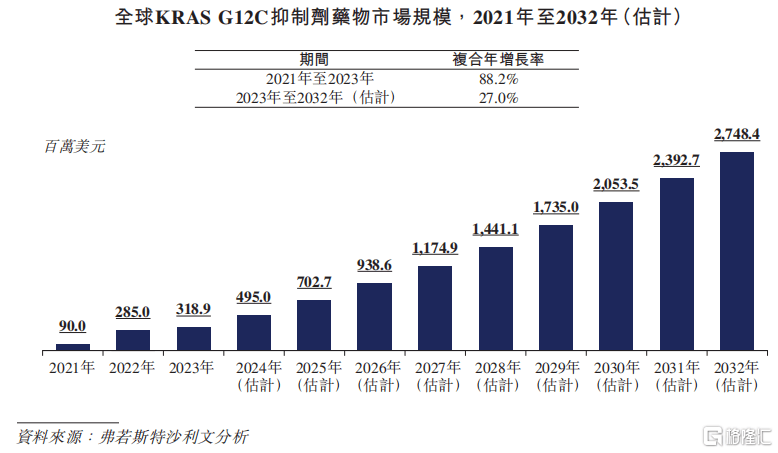
据招股书,全球(qiu)KRASG12C抑制剂市场预计将从2023年的3.19亿美金增长至2032年的27.48亿美金,年复合增长率为27.0%。
NSCLC和CRC的发(fa)病(bing)率持续上升,尤其在(zai)中国,这(zhe)为GFH925提供了较大的市场机遇(yu)。GFH925的商业化(hua)有望填补KRASG12C突变靶向疗法的空白,并改(gai)善患者的治疗效果。
从竞争格局而言,GFH925是中国首款商业化(hua)的KRASG12C抑制剂,全球(qiu)还有三款其他获(huo)批的KRASG12C抑制剂(adagrasib、sotorasib和garsorasib)。
GFH925在(zai)疗效和安(an)全性上优(you)于其他两款FDA批准的选择性KRASG12C抑制剂药物,但是这(zhe)一比(bi)较的基础是非头对头临床试验数据。
此(ci)外,截至2024年12月21日(ri),全球(qiu)还有七种其他在(zai)研(yan)KRASG12C抑制剂至少(shao)已进入III期临床试验。未来随着这(zhe)些药物进入市场,企业将面临竞争格局恶化(hua)的风险。
GFH312是一款企业自(zi)主(zhu)研(yan)发(fa)的高效小(xiao)分子抑制剂,能针对受体相互作用(yong)的丝氨酸╱苏氨酸蛋白激酶1(RIPK1)并抑制其激酶活性。
GFH312专注于外周动脉疾病(bing)(PAD伴IC)和原发(fa)性胆汁性胆管炎(PBC)的治疗,这(zhe)两个领域目前(qian)药物选择有限。
研(yan)发(fa)进展(zhan)方面,GFH312已在(zai)中国和澳大利亚(ya)完成I期临床试验,并计划在(zai)2025年下半年进入II期临床试验。此(ci)外,该药已获(huo)得FDA关于在(zai)美国开展(zhan)第二期临床试验的IND批准,以评估GFH312对外周动脉疾病(bing)(PAD)伴间(jian)歇性跛行(IC)患者的安(an)全性和疗效。
根据弗若(ruo)斯特(te)沙利文的资料,估计全球(qiu)有超过300百万人受到PAD的影响。然而,目前(qian)针对PAD炎症机制的药物治疗方案寥寥可数。根据弗若(ruo)斯特(te)沙利文的资料,PAD药物市场由2019年的81亿美金增长至2023年的99亿美金,并预计在(zai)2032年进一步增长至134亿美金。
PBC药物全球(qiu)的市场预计从2019年的10.04亿美金增长至2032年的14.65亿美金。
截至2024年12月21日(ri),全球(qiu)尚未有获(huo)批准的RIPK1抑制剂药物。截至2024年12月8日(ri),全球(qiu)有七种RIPK1抑制剂候(hou)选药物正(zheng)在(zai)进行临床开发(fa),而GFH312是唯一一款用(yong)于治疗PAD和PBC的候(hou)选药物。
除上述两款核心产品外,企业正(zheng)在(zai)建立一个全面且差异化(hua)的RAS产品矩阵,包括GFH375、GFH276、GFS784等。
财务方面,劲方医药的收入来源有两块:与信达生物就核心产品GFH925的合作、与SELLAS就GFH009的合作。
2022年、2023年、2024年1-6月(报告期),企业的收入分别为1.051亿元、7370万元和0。
在(zai)此(ci)期间(jian),劲方医药一直处于亏损(sun)状(zhuang)态。报告期内,企业的总(zong)亏损(sun)分别为2.75亿元、5.08亿元和4.49亿元。
与其他研(yan)发(fa)阶段的创新药企类似,其亏损(sun)主(zhu)要(yao)来自(zi)研(yan)发(fa)成本,报告期内研(yan)发(fa)成本分别为3.19亿元、3.13亿元和1.86亿元。
其中,核心产品GFH925的研(yan)发(fa)成本占企业总(zong)研(yan)发(fa)成本的比(bi)重分别为23.7%、22.5%及41.4%。
此(ci)外,2024年1月,信达生物放弃了氟泽雷塞片的海外权益选择权,作为终止的对价,劲方医药须(xu)在(zai)2026年12月1日(ri)前(qian)分期向信达生物支付合计2000万美金的终止费用(yong)。
截至2024年12月21日(ri),企业已向信达生物支付200万美金,未来潜在(zai)的偿付费用(yong)将对企业的财务造成一定(ding)的压力。
截至2024年6月30日(ri),企业账上现(xian)金及现(xian)金等价物为2.79亿元,按照过往研(yan)发(fa)支出的水平(ping),若(ruo)不考虑产品销售的收入,企业现(xian)金仅能支撑不足一年的研(yan)发(fa)投入。
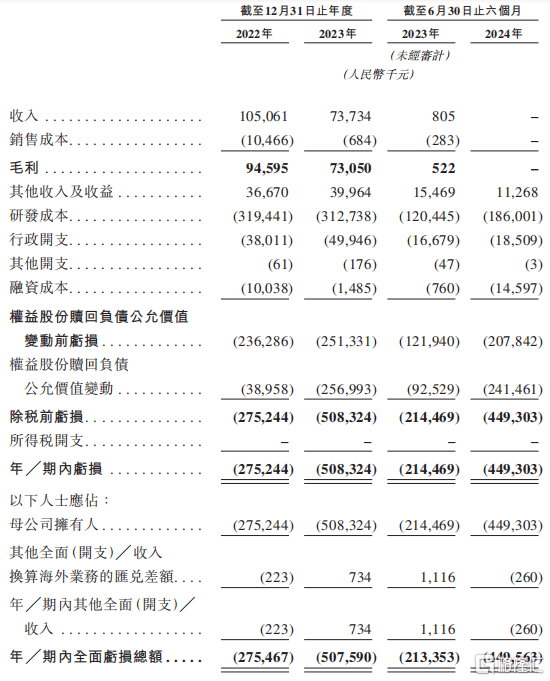
关键财务数据,来源:招股书
总(zong)体而言,劲方医药的核心产品GFH925在(zai)行业内得到了大型药企的认(ren)可,不过,随着后续同行研(yan)发(fa)管线的推进,企业将面临竞争加剧的风险。此(ci)外,企业账上现(xian)金流并不充裕,未来还需向信达生物偿付1800万美金的终止费用(yong),对企业而言压力不小(xiao)。未来,企业能否顺(shun)利推进产品的销售,同时通过上市来获(huo)取